2019年廣東省廣州市中考化學試卷
一、選擇題(本題包括20小題,每小題2分,共40分)注意:每道選擇題有四個選項,其中只有一項符合愿意.請用鉛筆在答題卡上作答.選錯、不選、多選或涂改不清的,均不給分.
1.(2分)做好垃圾分類,為綠色發展做貢獻。下列可回收垃圾主要成分為有機合成材料的是( )
A.舊報紙B.塑料瓶C.鋁制易拉罐D.玻璃瓶
2.(2分)“食在廣州”,下列廣州美食中富含蛋白質的是( )
A.增城遲菜心B.從化荔枝C.沙灣姜撞奶D.沙河粉
3.(2分)空氣是一種寶貴的資源,下列生產生活中用到的氣體不是來自空氣的是( )
A.作為燃料電池燃料的H2B.用于生產氮肥的N2
C.用于醫療急救的O2D.用于飛艇的He
4.(2分)下列過程中,發生了化學變化的是( )
A.干冰變成CO2氣體
B.從含SiO2的沙子中提煉高純Si
C.海水曬鹽
D.從潮濕空氣中分離出水
5.(2分)下列實驗操正確的是( )
A.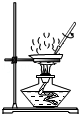 將蒸發皿直接加熱
將蒸發皿直接加熱
B.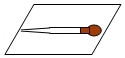 取液后的膠頭滴管平放在桌面上
取液后的膠頭滴管平放在桌面上
C.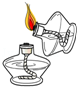 用燃著的酒精燈點燃酒精燈
用燃著的酒精燈點燃酒精燈
D.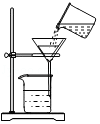 將混合液倒入過濾器過濾
將混合液倒入過濾器過濾
6.(2分)如圖為某反應的微觀示意圖,“![]() ”、“
”、“![]() ”各表示一種原子,下列說法不正確的是( )
”各表示一種原子,下列說法不正確的是( )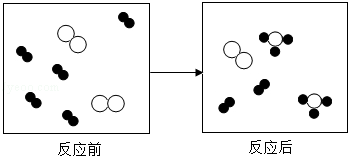
A.反應物是兩種單質B.反應物有剩余
C.該反應為化合反應D.該反應生成了多種產物
7.(2分)下列物質的使用能夠達到目的是( )
A.用明礬對水進行殺菌消毒
B.用堿液清洗水垢
C.用生石灰和水作為“自熱米飯”的熱源
D.用活性炭將硬水軟化
8.(2分)超氧化鉀(KO2)常備于急救器和消防隊員背包中,能迅速與水反應放出氧氣:2KO2+2H2O═2KOH+X+O2↑,關于此反應的說法不正確的是( )
A.X的化學式為H2O2
B.反應前后元素種類發生變化
C.反應前后氧元素化合價發生變化
D.反應前后物質狀態發生變化
9.(2分)下列物質的性質與用途均正確并相對應的是( )
| 性質 | 用途 |
A | 鋁在空氣中與氧氣反應生成致密氧化膜 | 鋁合金用于制作衛生間的置物架 |
B | 鎢的導電性好 | 鎢用于制作燈泡里的燈絲 |
C | CO2水溶液顯酸性 | CO2用作大棚蔬菜的氣體肥料 |
D | 氫氧化鈉能夠與酸反應 | 氫氧化鈉用于改良酸性土壤 |
A.AB.BC.CD.D
10.(2分)下列關于氯化鈉的認識,正確的是( )
A.組成:含有鈉和氯兩種單質
B.性質:與鹽酸類似,能與碳酸鹽反應
C.用途:可用于生產金屬鈉
D.生產:常用鈉與氯氣通過化合反應獲得
11.(2分)中國古代詩句中蘊含有很多化學原理,下列詩句的解釋不正確的是( )
| 詩句 | 解釋 |
A | 吳山開,越溪涸,三金合冶成寶鍔 | “寶鍔”的成分為合金 |
B | 遙知不是雪,為有暗香來 | 分子在不停地運動 |
C | 千淘萬漉雖辛苦,吹盡狂沙始到金 | 金的密度比沙大 |
D | 千錘萬鑿出深山,烈火焚燒若等閑 | 煅燒生石灰得到熟石灰 |
A.AB.BC.CD.D
12.(2分)燃料和能源與生活息息相關,下列說法正確的是( )
A.石油是一種清潔能源,也是一種可再生能源
B.炒菜時油鍋著火,應立即用水澆滅
C.“鉆木取火”的原理是通過摩擦生熱提高木材的著火點
D.燃氣灶火焰出現黃色,鍋底出現黑色時,可增大灶具進風口
13.(2分)25℃時,探究某固體物質的溶解性,實驗記錄如下表。下列實驗結論正確的是( )
編號 | ① | ② | ③ | ④ |
水的質量/g | 50 | 50 | 50 | 50 |
加入固體質量/g | 5 | 10 | 15 | 20 |
現象 | 固體完全溶解 | 固體完全溶解 | 剩余少量固體 | 剩余較多固體 |
A.實驗①所得溶液質量分數為10%
B.實驗②說明25℃時該物質的溶解度是20g
C.實驗③④所得溶液質量分數相同
D.實驗④所得溶液中含溶質20g
14.(2分)從地溝油中提煉生物柴油是垃圾資源化的方法之一。生物柴油主要成分是硬脂酸甲酯(C19H38O2),下列有關硬脂酸甲酯的說法正確的是( )
A.C、H、O三種元素的質量比為19:38:2
B.相對分子質量為(12×19+1×38+16×2)
C.C、H、O三種原子的個數比為12:1:16
D.氧元素的質量分數為![]() ×100%
×100%
15.(2分)煤和燃油的燃燒是造成空氣污染的重要原因,下列排放物能形成酸雨的是( )
A.SO2、NO2B.CO、CO2
C.煙塵D.未充分燃燒的汽油
16.(2分)下列物質混合后能夠反應,且有明顯現象的是( )
A.向氧化鐵粉末中滴入氫氧化鈉溶液
B.向稀硫酸中滴入稀氫氧化鉀溶液
C.將硫酸銨與熟石灰混合研磨
D.向澄清石灰水中滴入氯化鋇溶液
17.(2分)某微粒M的結構示意圖如圖,關于該微粒的說法正確的是( )
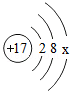
A.M的原子易失電子B.x只能為7
C.M為金屬元素D.x為8時,M為陰離子
18.(2分)下列物質與空氣充分混合后,遇明火不會發生爆炸的是( )
A.P2O5B.面粉C.鎂粉D.CH4
19.(2分)除去下列物質中混有的少量雜質(括號內為雜質),所用方法正確的是( )
A.Zn粉(Fe):用ZnCl2溶液浸泡,過濾
B.碳粉(MnO2):滴入H2O2溶液,過濾
C.NaCl溶液(Na2SO4):加入適量MgCl2溶液,過濾
D.CO2(H2O):通過盛有濃硫酸的洗氣瓶
20.(2分)下列實驗中,現象正確且可得到相應結論的是( )
| 實驗操作 | 現象 | 結論 |
A | 把硫在空氣中點燃,再伸進充滿氧氣的集氣瓶里 | 硫在空氣中燃燒發出淡藍色火焰,在氧氣中燃燒發出藍紫色火焰 | 硫在空氣中燃燒生成SO2,在氧氣中燃燒生成SO3 |
B | 在電解器的玻璃管中加滿水,接通直流電源 | 兩極玻璃管中有氣體生成,體積比是1:2 | 水是化合物,可分解 |
C | 高溫條件下,將CO通入Fe2O3粉末 | 黑色粉末變為紅色 | 可利用CO的還原性來煉鐵 |
D | 將帶火星的木條置于一瓶盛有氧氣的集氣瓶口上方 | 木條不復燃 | O2能支持燃燒 |
A.AB.BC.CD.D
二、(本題包括5小題,共30分)
21.(3分)地球大氣中存在氧氣(O2)和臭氧(O3)兩種含氧元素的單質,其中臭氧氧主要存在于15000﹣30000米的高空,能減弱高能量紫外線對地球表面的輻射。
(1)O3表示一個(填“原子”、“分子”或“離子”)
(2)高空中可發生轉化:2O3![]() 3O2,該變化屬于(填“物理”或“化學”)變化。
3O2,該變化屬于(填“物理”或“化學”)變化。
(3)鎂在氧氣中燃燒的化學方程式是。
22.(5分)氯化氫(HCl)是極易溶于水的無色氣體,其水溶液叫鹽酸。
(1)在充滿HCl氣體的試管中放入用石蕊染成紫色的干燥紙條,無明顯現象;再滴入水,現象是。
(2)向盛有NaHCO3粉末的試管中通入HCl氣體,無明顯現象;停止通氣,再加入少量水,現象是,發生反應的化學方程式是。
(3)畫出HCl氣體和鹽酸的微觀粒子組成示意圖,并進行必要的標注(水分子不用畫出)。
23.(5分)有一包白色固體樣品,可能含有NaOH、Na2CO3、K2SO4、BaCl2中的一種或幾種,為確定其組成,進行如下實驗:
步驟Ⅰ:取少量樣品于燒杯中,加足量水,充分攪拌,靜置,有固體剩余。
步驟Ⅱ:取步驟I所得上層清液于試管中,滴入幾滴酚酞溶液,溶液變紅色;再滴入過量稀鹽酸,無氣泡產生,紅色逐漸褪去,得到無色溶液。
步驟Ⅲ:取步驟Ⅱ所得溶液于試管中,滴入過量Ba(NO3)2溶液,無明顯現象。
根據上述實驗,回答下列問題:
(1)步驟Ⅱ中溶液的紅色褪去,發生反應的化學方程式是。
(2)分析上述實驗過程,關于樣品的組成,可以得到的結論是。
(3)若要進一步確定樣品的組成,還需進行的實驗操作是。
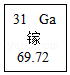
24.(7分)2019年是國際元素周期表年。俄國化學家門捷列夫在公布元素周期表時,就預言了當時還未發現的相對原子質最約為68的元素的存在,且性質與鋁相似,稱為“類鋁”。如圖是元素周期表中“類鋁”元素鎵的相關信息,請同答下列問題:
(1)鎵原子核外電子數為。
(2)金屬鎵與稀硫酸反應,產物中Ga的化合價為+3,反應的化學方程式是。
(3)高純氧化鎵廣泛用于生產半導體材料,其一種制備方法如下:
步驟Ⅰ:向含有硫酸的硫酸鎵溶液中通入氨氣(NH3),冷卻,生成Ga(NH4)(SO4)2固體。
步驟Ⅱ:在一定條件下灼燒Ga(NH4)(SO4)2固體,制得高純氧化鎵。
①Ga(NH4)(SO4)2中含有的帶電的原子團(根)是(填化學符號)。
②步驟Ⅰ反應的化學方程式是。
25.(10分)稀土金屬因其獨特的性能而被譽為“新材料之母”。稀土金屬釔的氧化物(Y2O3)廣泛應用于航空航天涂層材料,其顆粒大小決定了產品的質量。利用富釔稀土(含Y2O3約70%,含Fe2O3、CuO、SiO2等約30%)生產大顆粒氧化釔的一種工藝如圖: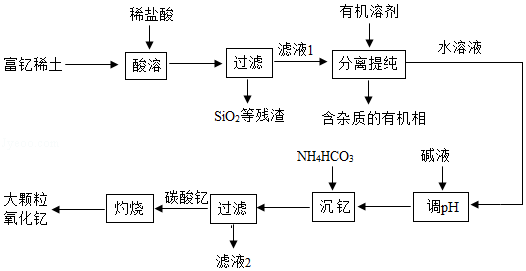
(1)氧化釔(Y2O3)中,Y元素的化合價為。
(2)“酸溶”過程中,氧化釔與鹽酸反應的化學方程式是。
(3)“分離提純”是為了除去濾液1中的(填化學式)。
(4)“調pH”時加入堿液使溶液的pH(填“增大”或“減小”)。
(5)碳酸釔灼燒分解的化學方程式是。
(6)為了獲得大顆粒氧化釔,某小組研究了條件對產品直徑的影響,相關數據如下(D50表示顆粒直徑):
實驗編號 | ① | ② | ③ | ④ | ⑤ | ⑥ |
沉淀反應溫度/℃ | 60 | 80 | 85 | 93 | 93 | 93 |
料液濃度/(g/L) | 30 | 30 | 30 | 30 | 40 | 40 |
灼燒溫度/℃ | 1100 | 1100 | 1100 | 1100 | 1100 | 1400 |
氧化釔D50/um | 6.00 | 21.65 | 35.99 | 38.56 | 35.99 | 61.54 |
分析上表數據,其他條件不變時,若將灼燒溫度均升高至1400℃,預期所得氧化釔D50最大的是(填實驗編號)。
三、(本題包括4小題,共30分)
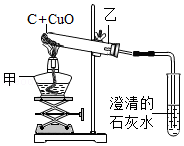
26.(4分)實驗室有如圖所示裝置,回答下列問題:
(1)連接裝置時,需根據導管的高度調節處的高度,再確定處的高度。(填“甲”或“乙”)
(2)結束實驗的操作是:先,再。
27.(7分)如圖1是實驗室制取CO2及進行性質實驗的部分裝置。
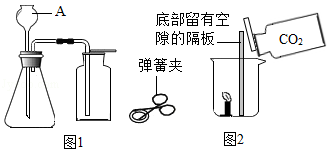
(1)CaCO3固體與稀鹽酸反應生成CO2氣體的化學方程式是。
(2)檢驗裝置氣密性,按圖連接裝置,先,再加水至A下端形成一段水柱,靜置,若觀察到,說明氣密性良好。
(3)加入藥品。添加塊狀CaCO3固體時,為避免打破錐形瓶,應將錐形瓶,再放入固體。添加鹽酸時,將稀鹽酸從(填儀器A的名稱)倒入錐形瓶至。
(4)如圖2所示,向放置有燃著的蠟燭的燒杯中倒入CO2,觀察到的現象是。
28.(9分)實驗室配制飽和澄清石灰水和質量分數為10%的氫氧化鈉溶液,并進行有關實驗。
下表是20℃時部分物質的溶解度數據。
物質 | Ca(OH)2 | NaOH | CaCO3 | Ca(HCO3)2 | Na2CO3 | NaHCO3 |
溶解度/g | 0.16 | 109 | 0.0065 | 16.6 | 21.8 | 9.6 |
(1)配制溶液。其中配制100g 10%氫氧化鈉溶液的基本步驟是:
稱取氫氧化鈉固體﹣量取水﹣溶解﹣裝瓶﹣貼標簽。
①稱取氫氧化鈉固體的質量g。
②已知水的密度為1g/cm3,用100mL量筒量取所需的水,畫出水的液面。
③裝瓶后貼標簽,在標簽上填寫:。
(2)進行性質探究實驗,20℃時,根據數據回答下列問題:
①向飽和澄清石灰水中通入CO2直至過量,先生成CaCO3,再轉化為Ca(HCO3)2,可觀察到的現象是。
②向10%氫氧化鈉溶液中通入CO2直至過量,先生成Na2CO3,再轉化為NaHCO3,可觀察到的現象是。
③理論上吸收4.4gCO2,需飽和澄清石灰水的質量至少為g,或需10%氫氧化鈉溶液的質量至少為g.(計算結果精確到個位)
![]()
29.(10分)已知金屬鈷(Co)的活動性與鐵相似,請預測氯化鈷(CoCl2)的化學性質,說明預測的依據,并設計實驗驗證。經查閱資料,鈷的化合物相關性質如下:
物質 | CoO | Co(OH)2 | CoCl2 | CoSO4 | Co(NO3)2 | CoCO3 |
在水中的溶解性 | 難溶于水的灰綠色固體 | 難溶于水的粉紅色固體 | 易溶于水形成粉紅色溶液 | 易溶于水形成粉紅色溶液 | 易溶于水形成粉紅色溶液 | 難溶于水的粉紅色固體 |
限選試劑:CoCl2溶液、(NH4)2CO3溶液、Na2SO4溶液、AgNO3溶液、NaOH溶液、稀硫酸、鎂條、銅片。
預測 | 預測的依據 | 驗證預測的實驗操作與預期現象 |
①能夠與含Ag+的 可溶性鹽反應 | CoCl2溶液中含Cl﹣, AgCl難溶于水。 | 取少量CoCl2溶液于試管中,,如果觀察到,則預測成立。 |
②能夠與 (填物質類別)反應 | 取少量CoCl2溶液于試管中,,如果觀察到,則預測成立。 | |
③能夠與 (填物質類別)反應 | 取少量CoCl2溶液于試管中,,如果觀察到,則預測成立。 |






